פורסם ב"Ynet".
פורסם ב"Ynet".
ההתקדמות הטכנולוגית בתחום האופטיקה והמחשוב ביחד עם פריצות דרך בתחום הנדסת מתכות, מאפשרת בעשור האחרון ביצוע של השתלות שיניים בעזרת שימוש במערכות אופטיות זעירות.
למי זה מתאים ומה היתרונות של השיטה?
השתלות שיניים: הדור הבא. ההתקדמות הטכנולוגית פורצת דרך בתחום האופטיקה והמחשוב ביחד עם פריצות דרך בתחום הנדסת מתכות, מאפשרת בעשור האחרון ביצוע של השתלות שיניים בעזרת שימוש במערכות אופטיות זעירות – (אנדוסקופ) ופיתוח שתלים "חכמים" (SMART IMPLANTS).
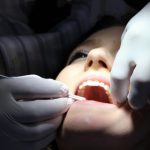
השימוש באנדוסקופים, כמו באזורים אחרים בגוף מאפשר שימוש בכירורגיה מזערית, ומונע במקרים רבים את הצורך בניתוחים קשים ומורכבים, הוא ממזער את הסיבוכים שלאחר הניתוח, ומאפשר ריפוי מהיר וטוב יותר.
אנדוסקופ הינו צינור חלול הכולל סיבי ראייה סיבי תאורה, מצלמה ויחידת טיפול, המאפשר ראייה של האזור הניתוחי על גבי צג טלוויזיה. האנדוסקופ לשתלים אשר פותח במחלקתנו מגיע עד לקוטר מינימלי של 0.9 מילימטר !! , ומכך שהחתך הניתוחי הינו מינימלי.
השימוש הראשון של אנדוסקופ כפי שמדווח בספרות הרפואית החל ב 1806 בווינה בעזרת מוביל אור וזכוכית מגדלת. עד שנת 1974 לא נעשה שימוש באנדוסקופ באזור הפנים וזו בשל מגבלות גודל אשר לא אפשרו החדרתו לאזורים קטנים בניתוח זעיר. האנדוסקופ לשתלים הינה מערכת אופטית ייחודית באיכות הראייה ובקוטר מזערי ובכך שהוא מכיל פתח המאפשר הכנסה של כלי עבודה במטרה לבצע פעולות כירורגיות מגוונות בראיה ישירה ללא צורך בפתיחה כירורגית נרחבת של האזור המנותח.
פריצת דרך טכנולוגית מאפשרת היום לאנדוסקופ להציג תמונה באיכות HD. ולמרות כל זאת העובי של האנדוסקופ הינו פחות מ-1 מילימטר. העלייה בתוחלת החיים באוכלוסייה מצריכה מתן מענה לאנשים עם חוסר שיניים. השימוש בשתלים כפתרון להשלמת שיניים החל בשנת 1970.
היום ידוע כי שימוש בשתלים הינו אחד הפעולות הכירורגיות הבטוחות ביותר עם אחוז הצלחה הגבוהה ביותר בתחום הרפואה בכלל. הצלחה של שתלים לטווח ארוך תלויה באיכות העצם אליה הוא מושתל, במינימום פגמים בעצם באזור ההשתלה, בהסרה של רקמות אשר אינן רקמות עצם ובתהליך הכנה קפדני.
מאז 1970 שוק השתלים עבר תהפוכות רבות והיום ידוע על למעלה מ- 1300 סוגים שונים של שתלים עם אחוזי הצלחה של כ 96-98% , נתון אשר מעמיד את השתלים כאחד הטיפולים הרפואיים המוצלחים ביותר.
טרם החדרה של שתל ללסת, המטופל בדרך כלל ישלח לבצע צילום סיטי אשר יאפשר לרופא המטפל להעריך את העצם באזור ההשתלה את איכות העצם ואת צפיפות העצם. נתונים אלו חשובים מאוד למהלך ההשתלה התקין ולהצלחתו של השתל לאורך שנים.
לצערנו ישנן מגבלות לצילום הסי טי המציג תמונה בגוונים של לבן שחור ואפור אשר יכול להשתנות בהתאם לסוג המדפסת שממנה הודפס הצילום, ובהתאם לסוג המכונה בה בוצע הצילום. לאחר שהרופא ביצע את הקידוח אליו אמור להיכנס השתל, כל ההחלטות של הרופא וכל המידע אשר יש לו לגבי המתרחש באותו האזור מתקבלות לפי תחושת בטן ולפי שימוש בכלים ידניים אשר אמורים לתת לו הרגשה על מה שקורה ומה נמצא בעומק הקדח.
פיתוחו של האנדוסקופ לשתלים מאפשר ראייה ברורה של החלל ללא מגבלת עומק, ללא מגבלת תאורה, וללא מגבלה של דימום מהאזור ובכך מאפשרת צפייה ישירה בסוג העצם, בצפיפות של העצם ומאפשרת לראות בעין את כל הקדח באזור ההשתלה.
ניתן להבחין בשאריות של זיהום, כלי דם ועצבים העוברים באזור, קרבה גדולה מדי לשיניים סמוכות או פריצה של עצם של הלסת ועוד. על המידע הזה נחוץ ביותר לדווח לרופא לצורך קביעת סוג השתל, פרוטוקול ההשתלה, ומאפשרת הצלחה של השתל לטווח ארוך.
טרם השימוש באנדוסקופ, כל המידע התקבל על סמך הסי טי ותחושת בטן, וללא ראייה ישירה. השימוש באנדוסקופ מאפשר ביצוע של הניתוח עם חיתוך מינימלי של החניכיים והעצם באזור ההשתלה, ובכך מקטין משמעותית את הכאבים ואת זמן ההחלמה לאחר הניתוח ומונע סיבוכים עתידיים.
שתל דנטלי הינו מעין "בורג" המיוצר מטיטניום אשר מוכנס לעצמות הלסת. על מנת לאפשר החדרה של השתל ללסת, יש צורך בעובי ורוחב מספק של עצם, שכן לא ניתן להחדיר את השתל לחלל ריק.
אנטומית, אצל כל בני האדם, בלסת העליונה באזור האחורי, קיים סינוס אשר הינו חלל אוויר המדקק את הלסת העליונה, כך שלא נשאר מספיק עובי של עצם בכדי להחדיר לתוכה שתלים. הניתוח הנפוץ היום בכדי להתגבר על בעיה זו הינו ניתוח להרמת סינוס, בו מבוצעת החדרה של חומרים (תחליפי עצם) באזור הסינוס על מנת לעבות את הלסת לצורך החדרת השתלים. ניתוח זה הינו מורכב מאוד ובעל פוטנציאל לסיבוכים משמעותיים (זיהום, דימום).
ניתוח זה דורש מיומנות גדולה עם סיכונים לא פשוטים, ומלווה בזמן החלמה ממושך. ניתוח זה דווח לראשונה בשנות השבעים, ומאז לא השתנה הרבה בנושא זה.
אחד המגבלות של הניתוח הוא הצורך לראות את הנעשה בו בראייה ישירה ומכך נגזר הצורך לבצע ניתוח נרחב עם חתך גדול והפשלה של כל החניכיים באזור.
פריצת דרך טכנולוגית בתחום הנדסת מתכות, אפשרה בחמש השנים האחרונות פיתוח של שתל דנטלי "חכם" (DIVA), המאפשר את ביצוע הרמת הסינוס דרך השתל עצמו, כולל החדרת חומרי מילוי ייעודיים, ותרופות. פותח מנגנון איטום המונע קשר בין הסינוס לחלל הפה.
היתרונות המשמעותיים בפיתוח של שיטה זו היא בכך שניתן לבצע את כל הפרוצדורה המורכבת של הרמת הסינוס דרך השתל בחתך מזערי ללא כניסה נרחבת לחלל הסינוס. הפעולה מבוצעת דרך אותו קדח המשמש את השתל ובכך מונעים סיבוכים היכולים להיגרם מניתוח הרמת הסינוס. ניתן להחדיר חומרי עצם תרופות וגם את האנדוסקופ דרך השתל לסינוס.
עולם הרפואה כולו נמצא במעבר לשימוש בכירורגיה מינימלית, ללא צורך בניתוחים גדולים ומורכבים. כניסתן לשוק הדנטלי של האנדוסקופ ושתלים ייעודיים כמו שתל ה- DIVA מאפשרים ביצוע של פעולות כירורגיות שעד לא מזמן דרשו ניתוחים מורכבים ומסובכים גרמו לאי נוחות וסבל למטופל ויכלו לגרום לסיבוכים משמעותיים.
ד"ר נעם ברוק, רופא בכיר, המחלקה לכירורגית הפה והלסתות, המרכז הרפואי ברזילי, אשקלון.
פרופ' עודד נחליאלי, מנהל המכון לרפואה וכירורגית הפה והלסתות, המרכז הרפואי ברזילי, אשקלון

פורסם באתר "Beok".
מתמודדת "האח הגדול 6" אורטל גושן, נאלצה לעזוב את הבית, כדי לעבור ניתוח לסרטן בבלוטת התריס.
עד כמה זה מסוכן? כל התשובות.
בתחילת השבוע כינסה מתמודדת "האח הגדול 6" אורטל גושן את חבריה לתכנית, וסיפרה להם כי עברה ביופסיה בבלוטת התריס, שתוצאתה מחייבת אותה לעבור ניתוח לכריתת בלוטת התריס. על מה בדיוק מדובר? האם נשקפת סכנה לחייה?
בלוטת התריס, שנקראת גם "בלוטת המגן" או התיירואיד (thyroid) נמצאת בתחתית הצוואר ומפרישה הורמון בשם תירוקסין, שאחראי על משק חילוף החומרים בגוף.
בהחלט כן. בישראל מדווח על 800 מקרים חדשים מדי שנה – מרביתם בנשים, הרבה מהם אצל נשים צעירות בעשורים ה-3 עד ה-5 לחייהן (בנות 20 ומשהו עד בנות 40 ומשהו). מבחינה זו, אורטל גושן בת ה-22, גם אישה וגם בעשור ה-3 לחייה – נופלת בדיוק לסטטיסטיקה.
בדרך כלל הוא מתגלה באקראי, כשהמטופלת ממששת גוש בצוואר. כאשר הגוש גדול, הוא עלול לגרום לתחושת אי נוחות באיזור, לצרידות, לקושי בנשימה או בבליעה – ואז זה יכול להיות הסימן המחשיד. כך היה אצל גושן, שסיפרה כי במהלך המיונים לתוכנית, חשה בנפיחות חשודה בבלוטת התריס. במקרה של חשד לגידול בגודל של כ-1 ס"מ ויותר או כזה שיש לו סממנים מחשידים, ההמלצה היא לבצע ביופסיה לבלוטה.
זאת בדיקה שנעשית במרפאת הרופא, באמצעות דיקור של מחט עדינה (FNA – Fine Needle Aspiration), ובמהלכה לוקחים בזהירות כמה דגימות קטנות של רקמה מתוך הבלוטה. הן נשלחות למעבדה, ושם מסתכל עליהן היסטולוג מתחת למיקרוסקופ, כדי לאבחן אותן. זה היה השלב שבו נכנסה אורטל לבית האח – אחרי הביופסיה ולפני הפענוח שלה.
רק ביופסיה מהווה הוכחה ודאית וחד-משמעית לקיום סרטן בבלוטה. גם אם חשדנו קודם, מכל מיני סיבות קליניות, שמדובר בגידול (נגיד: נפיחות בצוואר, חשד במישוש על ידי הרופא ותלונה על צרידות) – רק הביופסיה תגיד בוודאות שזה אכן גידול, ומאיזה סוג בדיוק.
כן, בהחלט. הסוג הנפוץ ביותר, קרצינומה פפילרית (Papillary thyroid carcinoma), נחשב לגידול שאיננו אלים במיוחד. בנשים צעירות מתחת לגיל 45, אנחנו מצליחים היום ברפואה להגיע כמעט ל-100% ריפוי שלו (ברפואה אין 100% מלא בשום דבר, כמובן). אצל נשים מבוגרות יותר, שיעורי הריפוי יורדים במעט.
בניגוד אליו, גידול שכיח הרבה פחות בשם קרצינומה אנאפלסטית (Anaplastic thyroid carcinoma) הוא אגרסיבי מאוד, מכפיל את גודלו כל כמה שעות (!!), והפרוגנוזה (התחזית להתפתחות המחלה) שלו היא עלובה מאוד, עם שיעורי ריפוי קטנים. קיימים עוד שני תת-סוגים של גידולי בלוטת מגן, שהם קטלניים פחות מקרצינומה אנאפלסטית – אבל לא עם סיכויי הבראה טובים כמו קרצינומה פפילרית.
הטיפול המרכזי הוא ניתוח לכריתת בלוטת המגן. מדובר בניתוח לא גדול באופן יחסי (לא ניתוח בטן לכריתת לבלב, למשל), שאורך כשעה עד שעתיים, ובמהלכו המנתח מנתק את הבלוטה מכלי הדם שמחוברים אליה, ומסיר אותה בעדינות מהצוואר. אם יש בלוטות לימפה חשודות באיזור (שייתכן והסרטן התפשט אליהן) – הן גם נכרתות. כעבור אשפוז של לילה עד שניים – החולה משוחררת לביתה.
כמעט. חוץ ממעקב קבוע למשך כל החיים, כדי לוודא שהמחלה לא חזרה (באופן תיאורטי, גם אחרי ניתוח בידיים מיומנות, עלול להישאר תא סרטני בודד באיזור – וממנו הסרטן עלול להתלקח שוב), בדרך כלל נהוג לתת טיפול חד פעמי ביוד רדיואקטיבי.
ממש ככה. תאי בלוטת התריס מאוד רגישים ליוד, ויכולים לרכז הרבה יותר יוד – מכל שאר התאים בגוף גם יחד. על היוד מרכיבים "טיל חכם" שהוא רדיואקטיבי, וכך הוא מחסל תאי סרטן. יוד רדיואקטיבי הוא מרכיב מרכזי בטיפול בסרטן הבלוטה כבר יותר מ-50 שנה, וכבר לפני 30 שנה פורסמו בספרות הרפואית מחקרים מדוקדקים שהוכיחו כי מי שנטלה את היוד הקטינה את סיכוניה לחזרת המחלה.
היוד ניתן למטופלת בשתייה, ובימים שלאחריו היא קורנת מעט – ולכן אסור לה לשהות במחיצת תינוקות, ילדים ונשים בהריון. גם מבני הבית עליה לשמור על מרחק מינימלי של 3 מטרים. אחרי כן היא חוזרת למרפאה, מודדים את הקרינה שנפלטת ממנה באמצעות מונה גייגר – והטיפול מסתיים.
ניתן לחיות היטב גם ללא בלוטת התריס – אבל צריך ליטול בזמן את התרופות וההורמונים שהמומחה לאנדוקרינולוגיה רושם למטופלת, ולהיות במעקב סדיר.
פורסם בפורטל "Beok"
לפני כשבוע נפטר מאמן קבוצת הכדורגל של ברצלונה, טיטו וילאנובה, מסרטן בלוטות הרוק. מהו סרטן בלוטות הרוק?
כיצד מאבחנים אותו ומהי טכניקת הטיפול החדשנית ביותר בתחום? כל התשובות בכתבה הבאה.
מאמן קבוצת הכדורגל של ברצלונה, טיטו וילאנובה, נפטר לאחרונה מסרטן בלוטת הרוק כשהוא בן 45 בלבד. במותו הוא מצטרף לכוכב ההיפ-הופ אדם יאוך, שנפטר לפני מספר חודשים מאותה המחלה.
מדי יום הגוף שלנו מפריש בין 1 ל-2 ליטר רוק, דרך 6 בלוטות גדולות (3 זוגות) ועוד מאות בלוטות קטנות, הפזורות במערכת הנשימה העליונה שלנו. הרוק מסייע להקל על בליעת ועיכול המזון, מאפשר לבלוטות הטעם לפעול (בלי רוק – פשוט לא נרגיש בטעמו של האוכל) ומגן על השיניים.
מרבית הגידולים בבלוטות הרוק מופיעים בבלוטות הגדולות ביותר – "בלוטת בת האוזן" או ה"פרוטיד" (parotid). הבלוטות הללו נמצאות בשני צידי הראש שלנו, קדמית ומתחת לאוזן (הן אלו שמתנפחות במחלת החזרת) – באחת מ-2 הבלוטות הללו התגלה הגידול אצל וילאנובה.
הרוב המוחלט (80%-90%) של הגידולים בבלוטות בת האוזן הם שפירים (לא סרטניים), ומיעוטם – ממאירים (כלומר: סרטניים). בישראל מדווח על כ-100 מקרי סרטן חדשים מסוג זה מדי שנה.
מה גורם לסרטן בלוטות הרוק? מדוע הוא הורג גברים צעירים? למדע ולרפואה עדיין אין תשובות מספקות לשאלות הללו. ידוע לכל כי עישון טבק מגדיל את הסיכון לסרטן הריאות וכי צלילה בקישון המזוהם מגדילה את הסיכון לכמה סוגי סרטן – אך עדיין לא ידוע מה גורם לסרטן בלוטות הרוק או אפילו מה מעלה את הסיכון ללקות בו.
במחקר שבוצע בארץ לאחרונה, נצפתה עלייה בשכיחות סרטן הפרוטיד ב-10 השנים האחרונות, והועלתה השערה ששימוש בטלפונים סלולריים אחראי לעלייה זו. השערה זו טרם הוכחה, והשפעת הקרינה הסלולרית על התפתחות סרטן עודה נמצאת במחלוקת בקרב המומחים בתחום. באופן כללי, סרטן בבלוטות הרוק מהווה 1% מהסרטנים ו-7% מהסרטנים באזור הראש והצוואר.
אבחון סרטן בלוטות הרוק מתבצע בדרך כלל בעקבות סימנים קליניים (כמו נפיחות או גוש באזור), וכולל בד"כ ניקור (FNA – Fine Needle Aspiration) כדי לבצע ביופסיה. דימות, ובייחוד MRI, יעיל בהדגמת רקמות רכות, ולכן מועדף על פני CT בתהליך האבחון של גידולי פרוטיד.
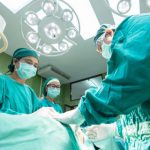
הטיפול המרכזי (ופעמים רבות הבלעדי) בגידולי בלוטת הרוק – הן השפירים והן הממאירים – הוא ניתוח לכריתת הבלוטה. הכריתה נעשיית בהרדמה כללית תחת ניטור עצב הפנים שנמצא בסיכון בניתוח (אם כי נמוך בד"כ). במקרים נבחרים מוסיפים לאחר הניתוח טיפולי קרינה (רדיותרפיה).
גם גידולים שפירים מהווים התווייה לניתוח לכריתת הבלוטה, וזאת משום שהם עלולים להפוך לממאירים ברבות השנים (כלומר, לעבור "התמרה סרטנית"). לכן מקובל להמליץ על כריתתו בשלמות של כל גידול שמתגלה בבלוטת הרוק.
לאחרונה פותחה טכניקה חדשה המציעה חתך מינימלי (Mini Incision) לאורך מתווה האוזן, שאינו מתמשך עד קו השיער
עד כה, הטכניקה הסטנדרטית בניתוח להסרת בלוטת הפרוטיד הייתה בשיטת "חתך בלייר" (Modified Blair Incision). בשיטה זו, המנתח מבצע חתך מאזור האוזן ולאורך קו הלסת ועד לצוואר, על מנת לחשוף עצבים חשובים בפנים כדי להימנע מלפגוע בהם במהלך הסרת הבלוטה.
למרות שהניתוח בשיטה זו מבוסס ויעיל, לאחרונה נבחנת מחדש טכניקת הניתוח משיקולים אסתטיים (שהרי הניתוח הוא בפנים, וצלקת עלולה לבלוט), וכיום קיימות שיטות חתך חלופיות.
טכניקה חלופית כזו, היא חתך שמבוצע בסגנון "מתיחת פנים" (facelift incision – FLI). חתך כזה נמשך מהגבול העליון של האוזן, לאורך מתווה האוזן ועד לאזור אחורי האוזן והראש. שיטה זו צברה פופולריות רבה בשל יתרונותיה הקוסמטיים, למרות שהחתך המבוצע אינו בהכרח קצר יותר מהטיפול הסטנדרטי.
לאחרונה פותחה טכניקה חדשה המציעה חתך מינימלי (Mini Incision) לאורך מתווה האוזן, שאינו מתמשך עד קו השיער. שיטת "מיני החתך" הזו יעילה באותה מידה של הניתוח הסטנדרטי ואף מציעה יתרונות העולים על הטכניקות האחרות: החלמה מהירה יותר, קיצור משך האשפוז והקטנת הסיכויים לצלקות ונפיחות באזור החתך.
למרות היתרונות הקוסמטיים של הטכניקות החלופיות הללו, מנתחים רבים עדיין נרתעים מלנתח באמצעותן כשמדובר בהסרת גידולים בפרוטיד, מחשש לפגוע בעצב הפנים. יש להדגיש שהניתוח בשיטות אלו איננו מסוכן יותר, אך הוא בהחלט דורש מיומנות וניסיון של המנתח. יחד עם זאת, קיימות קליניקות ייעודיות המתמחות בניתוחים להסרת בלוטות רוק, בהן שיטת החתך המינימלי נפוצה.
הפרוגנוזה (תחזית לריפוי המחלה) תלויה מאוד בשלב שבו המחלה התגלתה (מ-1 – הקל ביותר; ועד 4 – כולל גרורות מרוחקות). כמובן, ככל שמתגלה מחלה קטנה יותר ובשלב מתקדם פחות- כך גדלים סיכויי הריפוי והפרוגנוזה חיובית יותר.
הימנעות מהישנות הסרטן (התפתחות סרטן בבלוטה לאחר תהליך של ריפוי והחלמה מהסרטן הראשוני) היא השיקול המרכזי החשוב ביותר בטיפול בחולים שעברו ניתוח להסרת הפרוטיד, ואמנם נדיר למצוא בה הישנות של גידול שפיר. הישנות הגידול משפיעה על שיעורי ההישרדות ארוכת הטווח של החולים.
סיכוי נמוך לחזרה של הגידול לאחר החלמה מהמחלה, מגדיל את שיעורי ההישרדות ארוכת הטווח. שיעור זה תלוי בגורמים נוספים כגון: סוג הגידול, ביכולת של הגידול לשלוח גרורות ובשלב שבו הוא נמצא בעת הניתוח.
הנתונים הכלליים לגבי כל החולים בכל השלבים, להישרדות ל-5 שנים מיום האבחון עומדים על 62% (היינו, כמעט שני שלישים מהחולים ימצאו את עצמם בחיים – 5 שנים לאחר שאובחנו עם סרטן בלוטות הרוק). הנתונים לגבי חולים שאצלם הייתה חזרה (הישנות) של המחלה לאחר הניתוח והטיפולים נמוכים יותר, ועומדים על הישרדות של 37% ל-5 שנים.

פורסם באתר "דוקטורס אונלי".
"לא תמיד חייבים לרוץ לנתח גידולי בלוטת המגן של פחות מ-1 ס"מ"
כך עולה מכנס החברה לכירורגיית ראש-צוואר, שנערך בחודש שעבר, בו הוצגו קריטריונים סונוגרפיים מסויימים המאפשרים להימנע מניתוח.
גידולים בבלוטת המגן (התיירואיד) הם אחד מסוגי הסרטן השכיחים ביותר, עם 800 חולים חדשים שמתגלים בישראל בכל שנה. ההסתמנות הקלאסית של הגידול היא גוש לא רגיש, שנע בבליעה, וממוקם בחלק האמצעי-תחתון של הצוואר. על פי הפרוטוקולים הנוכחיים, יש לבצע אצל מטופל שנתגלה אצלו גידול תיירואיד כריתה רדיקלית של הבלוטה (Thyroidectomy) ולאחר מכן לטפל בו באמצעות מתן יוד רדיואקטיבי באופן פומי בטיפול ביתי, וכמובן לעקוב אחר סימנים להישנות.
על פי הגישה החדשה, שמבוססת על נתונים מחקריים, חולים עם גידולים ממאירים בבלוטת התריס שקטנים מ-1 ס"מ ומציגים את אותם סממנים בדימות – יכולים להימנע מניתוח ולהסתפק במעקב בלבד, ואפילו אין צורך לשלוח אותם לביופסיה.
"זוהי גישה חדשה יחסית", מדגיש ד"ר חפץ, "ויש צורך לבחון אותה לאורך זמן, אם כי התוצאות הראשוניות שלה בהחלט נראות מבטיחות, ועשויות למנוע ניתוחי צוואר מיותרים".
על פי גישה זו, גם מקרה של הישנות מיקרוסקופית של גידול כזה (כלומר: גידול תיירואיד שבעקבות גילויו נכרתה בלוטת המגן כולה, ולאחר מכן הוא חזר מיקרוסקופית לבלוטת לימפה), אינו מחייב ביצוע של ניתוח מיידי לכל חולה (ואפילו לא ניקור) – ומספיק לבצע מעקב אחריו.
הקלינאים שהרצו בכנס הדגישו, כי גם גישה זו היא חדשה ומחקרית, וטרם נכנסה לפרוטוקול הטיפולים המחייב. לדבריהם, יש לבחון אותה בזהירות הראויה. כיום, על פי הפרוטוקולים הנוכחיים, זיהוי של הישנות גידול מליגני לאחר ניתוח, מחייבת ביצוע של ניתוח חוזר, כדי לנקות את האיזור מתאי גידול ומגרורות מקומיות.
תחום מעניין נוסף שגם בו, כך נראה, ניתן לחסוך מהחולה ביצוע של פרוצדורה פולשנית, הוא סרטן האפיתל הקשקשי, שחזר לאחר טיפולי כימותרפיה ורדיותרפיה משולבים.
מההרצאות שניתנו בכנס, עולה כי גם אם יש רושם קליני של גידול שארתי בצוואר (בעקבות מישוש או דימות), אין לשלוח את החולה מייד לבצע דיסקציה צווארית, ומומלץ, קודם לכן, לבצע PET-CT. במידה ואין בגוש הצווארי קליטה – ניתן לחסוך מהחולה את ביצוע הניתוח.
בכנס, שנערך בים המלח בחודש שעבר, השתתפו בכירי הרופאים בתחום בישראל, לצד מומחים בעלי שם עולמי, כולל שלושה נשיאים לשעבר של החברה לכירורגיה ואונקולוגיה של ראש צוואר בארה"ב. אלו כללו את: ג'אטין שאה (Jatin Shah), מנהל המחלקה לניתוחי ראש-צוואר ב"ממוריאל סלואן קייטרינג" בניו יורק; אשוק שאשא (Ashok Shaha), מנתח בכיר באותה מחלקה; ופרופ' ג'יזס מדינה (Jesus Medina) המכהן גם כיו"ר ה-Triological Society היוקרתית (המאגדת רופאים העוסקים בלרינגולוגיה, רינולוגיה ואוטולוגיה).

פורסם באתר "Doctors".
לאחר שנים ארוכות של התמודדות עם המחלה, נפטר אתמול השחקן המפורסם. המחלה נובעת לרוב מעישון. כיצד מאבחנים סרטן גרון וכיצד מטפלים בו?
השחקן והקומיקאי הישראלי ספי ריבלין הלך אתמול (ג') לעולמו, בתום מלחמה ארוכה במחלת הסרטן. ריבלין היה בן 66 במותו. בשנים האחרונות המשיך להופיע במתכונת מצומצמת, וגם כשהתקשה לדבר, דמותו הייתה חלק מהחיים הציבוריים בישראל, עד שנדם קולו.
כיצד מאבחנים את סרטן הגרון?
"חולים רבים מגיעים לרופא בפעם הראשונה בגלל צרידות שלא עוברת", מסביר ד"ר אבי חפץ, מנהל היחידה לכירורגיה ואונקולוגיה של ראש צוואר באסותא ויו"ר לשעבר של החברה לכירורגיה ואונקולוגיה של ראש צוואר. "ההשפעה על הקול ניכרת מכיוון שהגידול שכיח באזור מיתרי הקול. כדאי להגיע לאבחון מוקדם ככל האפשר, מכיוון שבשלב זה שיעור הצלחת הטיפול עומד על כ-90 עד 95 אחוז. לעומת זאת, כשחולה מגיע עם גידול נרחב יותר, סיכויי ההחלמה הם מתחת ל-50%".
לדברי ד"ר חפץ, סוגי הטיפול משתנים לפי השלב שבו התגלה הסרטן. בשלב הראשוני ניתן לכרות את הגידול באמצעות לייזר ללא קרינה וללא חתך. בשלב זה כאמור סיכויי ההבראה המלאים גבוהים ואיכות הקול בדרך כלל תישמר.
"בשלב מעט מתקדם יותר שבו קשה לכרות את הגידול בשלמותו באמצעות הלייזר, הטיפול המומלץ הוא באמצעות קרינה, עם או בלי כימותרפיה. בצורה זו ניתן לחסוך את הצורך בניתוח של כריתת גרון חלקית או מלאה. בשלבים מתקדמים מוסיפים כימותרפיה או טיפולים ביולוגיים, ושילוב זה נועד לחסוך כריתת גרון מלאה".
בשלב המתקדם ביותר של המחלה, כאשר טיפול קרינתי כימותרפי לא מצליח להתמודד עם המחלה, ניתן לכרות את כל קופסת הקול. בניתוח זה נעשה חיבור של קנה הנשימה לצוואר, כך שהחולה נושם ישירות לקנה ולריאות. מכיוון שכריתה כזו פוגעת ביכולת הדיבור, כיום ניתן להשתיל תותב דיבור בקיר המשותף בין הקנה לוושט. לאחר אימון קצר המטופל מצליח לדבר בצורה מובנת, אפילו בטלפון. אף שכריתת גרון היא הפתרון הכי קיצוני לבעיה, מדובר בניתוח מצוין מבחינה אונקולוגית, שנותן לחולה סיכוי לשרוד את מחלת הסרטן. במקרה שישנן גרורות מרוחקות, לרוב בריאות, הטיפול הוא כללי-כימותרפי וסיכויי ההחלמה למרבה הצער נדירים ביותר.
איך למנוע את המחלה?
"כמו בכל גידול סרטני, הטיפול הטוב ביותר הוא הטיפול המונע", מסביר ד"ר חפץ, "כלומר במקרה של סרטן הגרון – בעיקר הימנעות מעישון". לפי הסטטיסטיקה, רוב החולים שלוקים בסרטן הגרון מעשנים או עישנו בעבר. העישון מגביר את הסיכון לסרטן הגרון, מערכת הנשימה העליונה והריאות פי 5 עד 15, ועישון בשילוב אלכוהול אף מעלה את הסיכון.

פורסם בעיתון "הארץ".
אמצעים טכנולוגיים מתקדמים מאפשרים לאחרונה פתרון ניתוחי לדלקות של הסינוסים הממוקמים במצח ולגידולים המתפתחים בהם.
ואתד, בן 36, בילה מחצית חייו בניתוחי אף וסינוסים. בגיל 18 עבר את הניתוח הראשון בשל קשיי נשימה. זה היה ניתוח לפתיחת סינוסים וכריתת פוליפים. כמה חודשים אחר כך הוא התלונן על כאבים במצח ועבר סריקת סי-טי, שבה התגלה כי הוא סובל מדלקת בסינוסים הפרונטליים (המצחיים). הוא עבר שני ניתוחים נוספים בעזרת אנדוסקופ (סיב אופטי), בניסיון לפתוח את הסינוסים החסומים, שהסתיימו ללא הצלחה. הניתוח הרביעי נעשה בגישה חיצונית. כלומר, באותו ניתוח בוצע חתך בקרקפת, נכרתה דופן העצם הקדמית של הסינוס, הסינוס נוקה מהדלקת ומולא בשומן שנלקח מהבטן.
ואתד חש הקלה, אבל היא היתה זמנית. כעבור זמן לא רב שוב התלונן על כאב במצח. הוא גם שם לב שעינו השמאלית בולטת והתלונן על ראייה כפולה. בבדיקת סי-טי שוב נראתה דלקת בסינוסים. בצד שמאל פרצה הדלקת לתוך ארובת העין ודחקה את העין לפנים.
מיכל, בת 32, סבלה שלושה חודשים מכאב חד שאינו מרפה בצד הימני של המצח, שהקשה עליה לתפקד. בסריקת סי-טי נראה בסינוס הפרונטלי הימני גידול המכיל בעיקר רקמת עצם. היא קיבלה טיפול אנטיביוטי, אבל לא חלה כל הטבה במצבה.
אלדד, בן 28, עבר שני ניתוחים אנדוסקופיים בשל סינוסיטיס עיקש, אבל הכאב לא חלף. לאחר כמה חודשים התאשפז בשל זיהום שהתפשט מהסינוס לעין. הוא נזקק לניתוח דחוף, שבו שיתפו פעולה מנתח אף-אוזן-גרון ומנתח ארובת העין, שניקזו את הזיהום. בתחילה הורגשה הקלה, אבל מקץ כמה חודשים הגיע אלדד שוב לבית החולים, עם כאב עז במצח. בסי-טי נצפה תהליך זיהומי בחלקו הצדי והמרוחק ביותר של הסינוס הפרונטלי.
שלושת המטופלים הללו סבלו ממחלה דלקתית או מגידול בסינוס הפרונטלי. למחלות אלה אין תרופה וגם ניתוחים סטנדרטיים אינם נותנים להן מענה יעיל.
הסינוסים, המכונים "מערות האף", ממוקמים במצח, מתחת לעיניים ומאחוריהן. אלה חללי אוויר בתוך הגולגולת, המחוברים לאף ומקבלים דרכו את אספקת האוויר. סינוסים מקטינים את משקל הגולגולת, משמשים תיבת תהודה לקול ורקמת הרירית המצפה אותן מחממת ומנקה את האוויר שאנו שואפים. לעתים, כתוצאה מחסימה מכנית, הצטננות שמסתבכת בזיהום חיידקי, התקף אלרגיה או רגישות לפטריות שנשאפות מהאוויר, עלולה להתפתח תגובה זיהומית שנקראת סינוסיטיס.
במרבית המקרים חולפת המחלה מעצמה או באמצעות תרופות. לעתים אפשר להציע למטופל ניתוח אנדוסקופי של האף והסינוסים, המבוצע דרך הנחיריים, ללא חתכים חיצוניים. מיקומם של מרבית הסינוסים מאפשר הגישה קלה וישירה יחסית. הסינוס הפרונטלי שונה: מיקומו הנסתר – מעל העין וקדמית למוח, זווית הגישה הלא נוחה והווריאציות האנטומיות השונות, מרתיעים מנתחים מלבחור בגישה אנדוסקופית ותכופות הם גוררים המלצה לניתוח בגישה חיצונית.
הגישה האנדוסקופית המסורתית לסינוס הפרונטלי מסתפקת בחשיפה או בהרחבה מוגבלת של פתחו. היות שבמרבית המקרים תוכן הסינוס המודלק נוזלי, די בפעולה זו. הבעיה נעשית מורכבת יותר אם, כמו אצל החולים שהוצגו, את הסינוס חוסמת רקמת צלקת נוקשה בעקבות ניתוחים קודמים; אם יש צורך להסיר מהאזור גידול; או אם התהליך הזיהומי נמצא בפינה מרוחקת של הסינוס.
בשנים האחרונות הולכת ומשתפרת מיומנות הגישה האנדוסקופית לסינוס הפרונטלי. ניתוח שהמציא מנתח אמריקאי, שפותח ושוכלל על ידי מנתח גרמני ומנתח אוסטרלי, חולל מהפכה בתחום.
בניתוח זה מתבצע באופן אנדוסקופי, דרך חללי האף, חיבור של חללי הסינוסים הפרונטליים על ידי כריתת רצפתם המשותפת והמחיצה שביניהם, כך שבסוף הניתוח נוצר ניקוז מרכזי משותף וגדול לשניהם. בניתוח מאפשר הפתח הגדול נגישות ניתוחית משופרת. במקום איטום וביטול הסינוסים בניתוח החיצוני, משמרים את ייעודו של הסינוס הפרונטלי כחלל פתוח המקבל אוורור דרך האף. בנוסף, ניתן בקלות להחדיר אנדוסקופ דרך האף ולסקור את החלל הניתוחי. ביצוע נאות ונטול סיבוכים מחייב מיומנות וטכנולוגיות מתקדמות.
ואתד ומיכל עברו את הניתוח בשיטה זו. אצל אלדד הוחלט ליישם שיטה חדשנית אחרת. האתגר היה להגיע אל המוקד הזיהומי הממוקם הרחק בקצה הסינוס הצדי, שאליו כלי ניתוח קונוונציונליים אינם מגיעים. לצורך זו נמצאה מתאימה מערכת sinuplasty. מפתחי שיטה זעיר-פולשנית זאת יישמו את הטכנולוגיה של צנתורי לב על הסינוסים: בפעולה מרחיבים את פתחי הסינוסים באמצעות בלונית, שאחר כך נשלפת מהאף.
הפעולה מתאימה לחולים שפתחי סינוס צרים הם המקור לבעיותיהם. הפעולה אינה כרוכה בחיתוך או בפגיעה באיברים בריאים, וזמן ההחלמה לאחריה קצר. אלדד היה מועמד טבעי לשיטה זו, שכן אצלו התעורר צורך להרחיב פתח אחד במקום שכלים רגילים אינם מגיעים אליו. שלושת החולים שוחררו לביתם למחרת הניתוח, ואחרי חצי שנה הם אינם סובלים מכאבים.
חשוב לזכור שלא כל כאב מצחי מקורו בסינוסיטיס, וצריך לברר את הסיבה בבדיקה אצל רופא אף-אוזן-גרון. במידה שמאובחן סינוסיטיס, המיומנות הניתוחית והטכנולוגיה הקיימים כיום מאפשרים פתרון אנדוסקופי במרבית המקרים, כולל המורכבים שבהם.

פורסם באתר "Ynet"
מתח נפשי, שפעת וגם נשימה לא נכונה עלולים להותיר אותנו מחוסרי קול רגע לפני פגישה חשובה בעבודה או הופעה. מה עושים כשהקול מתחיל להיחלש והופך לא יציב? מומחה מייעץ.
זה הסיוט הגדול ביותר של כל מי שקולו הוא המקצוע שלו: אמן מתכונן להופעה חשובה ויודע שקהל רב מצפה לו וששאר חברי המופע תלויים בו. ואז, יום לפני המופע, הקול מתחיל לבגוד. הוא חש עקצוצים וכאבים בגרון, קולו חלש ולא יציב. כעת זה ברור – הוא לא יוכל לעמוד בהופעה.
לפני כשבוע מצאה את עצמה במצב הזה הזמרת הצעירה רודי ביינסין, המתמודדת בתוכנית "The Voice". בבדיקה דחופה של מיתרי הקול נמצא שהם אדומים ונפוחים עם סימני דלקת וגירוי, כתוצאה משפעת קלה לצד אימוץ המיתרים בחזרות האינטנסיביות לתוכנית. שילוב של טיפול תרופתי והנחיות להתנהגות קולית בזמן המחלה אפשרו לה לחזור בזריזות לתלם, להמשיך להתחרות ולהופיע עם קול צלול וחזק.
למה זה קורה? מיתרי הקול הם צמד שרירים המצופים במספר שכבות עדינות ומורכבות, אשר מתפקדים בהרמוניה להפקת צלילים שתלויים מצד אחד בזרימת האוויר מכיוון הריאות, ומהצד השני מושפעים מתיבת התהודה הטבעית שלנו בלוע וחללי האף. מעבר לכך, הפקת קול היא תהליך רגשי וביטוי אינדיבידואלי. איכות הקול טובה כשרמת הביטחון והנוחות של האמן גבוהה, ובאופן דומה ירודה כשהוא חש חרדה.
1. בעיות מכניות
אלו הן בעיות המשפיעות על התפקוד של מיתרי הקול: מחלה ויראלית שתסמיניה הם כאבי גרון, שיעול וצינון יכולה לערב גם את מיתרי הקול ולגרום לצרידות פתאומית וקשה, מלווה באטימות של האף והאוזניים ובהרגשה כללית רעה.
עישון גורם לנזק מצטבר, אשר יכול במקרים מסוימים לגרום להפרעה פתאומית בקול בשל בצקת או חספוס של המיתרים.
מאמץ יתר בהפקת קול בזמן הכנות למופע או בזמן מאמץ קולי לא אחראי יכול לגרום לקרע מיקרוסקופי במיתר ולדימום, אשר יתבטא באובדן קול פתאומי ובכאבים בגרון. ייתכן גם שילוב של כל הגורמים הללו.
2. בעיות תפקודיות
מדובר במקרה שבו המיתרים עצמם בריאים ותקינים, אך המערכת אינה עובדת בצורה מתוזמנת ויעילה. לחץ מוגזם על המיתרים, שימוש לא נכון בשרירי הנשימה והסרעפת, תהודה לא יעילה – כל אלו יכולים לגרום לקול חלש, להתעייפות קולית ולכאבים בזמן הפקת קול.
3. סיבות רגשיות
אמן החושד שיש לו הפרעה במיתרי הקול, במיוחד לקראת הופעה חשובה, סובל ממתח נפשי הולך ומתעצם הגורם לפגיעה נוספת בתפקוד הקולי. לעתים התגובה הרגשית היא הבעיה העיקרית הגורמת לאמן להפסיק לתפקד קולית.
במקרה של איבוד קול פתאומי, מדובר בדרך כלל בתופעה זמנית וחולפת שניתן לטפל בה ביעילות בליווי רופא המומחה למחלות מיתרי הקול.
ראשית, יש לעבור בדיקה יסודית של מיתרי הקול באמצעים המתקדמים הקיימים כיום במרפאות המתמחות. שימוש בסיב אופטי גמיש או קשיח והקלטת הבדיקה בווידאו הכרחיים לאבחון ולהדרכת האמן.
לאחר מכן, החשוב ביותר הוא להרגיע את האמן, להראות לו את מיתרי הקול שלו ולהסביר את מהות הבעיה. פעמים רבות, הסבר שהמיתרים תקינים והדגמת פעילותם הנורמלית תוך התבוננות משותפת בסרט הבדיקה ישרו על המטופל רוגע ויובילו להקלה שתאפשר חזרה לתפקוד קולי בידיעה שלא נגרם נזק בלתי הפיך.
אם מדובר בהפרעה תפקודית, ניתן להדריך את הזמר או את השחקן להשתמש בשרירי הקול שלו באופן נכון, שלא יגרום להתעייפות ולשחיקה.
אם מאובחנת מחלה כגון דלקת ויראלית של המיתרים, בצקת או דימום יש להגיב בטיפול מיידי בהתאם למקרה.
להירגע ולנוח. תנו למיתרים לנוח ככל שניתן והימנעו מדיבור מיותר לפני הופעה.
לחמם את הקול. ערכו חימום מסודר וחזקו את הביטחון שלכם בקול.
שתו הרבה מים לקראת ההופעה. מים מרגיעים את הגרון, מגבירים את הלחות ומונעים יובש וחימום מקומי.
ליטול תרופות מתאימות. בכל הנוגע לטיפול תרופתי יש להפעיל שיקול דעת ולהתייעץ עם מומחה. חשוב לדעת שתרופות נגד אלרגיה, נוגדי גודש ומייבשים עשויים לפגוע באיכות הקול. אנטיביוטיקה לרוב אינה נחוצה, וגם טיפול בסטרואידים צריך להתבצע בשיקול דעת ובזהירות רבה.
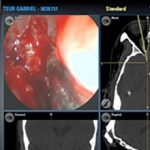
מערכת ניווט ("GPS") בניתוחים אנדוסקופים של האף והסינוסים
לעיתים, גם הכיסוי התרופתי הרחב והממושך ביותר אינו פותר את תסמיני החולה הלוקה בסינוסיטיס. במצבים אלה יש לשקול ניתוח אנדוסקופי של האף ומערות הפנים (ESS – Endoscopic Sinus Surgery), אשר כבר ביסס את מעמדו כטיפול הכירורגי המקובל והמועדף לבעיה רפואית זו. הניתוח כולו מבוצע דרך הנחיריים, ללא צורך בחתכים חיצוניים. במהלך הניתוח מוחדר דרך אחד הנחיריים סיב אופטי קשיח המחובר למוניטור שמציג את השדה הניתוחי בהגדלה. במקביל מתבצעות דרך אותו נחיר פעולות כירורגיות כגון: שאיבה, חיתוך או הסרה של רקמה רכה או גרמית (דפנות עצם) באמצעות כלים ייעודים.
לשיטה זו יתרונות ברורים: דיוק רב, התערבות מינימלית, הימנעות מפגיעה באיברים בריאים שאינם מהווים חלק מהבעיה הרפואית, היעדר חתכים חיצוניים והחלמה מהירה יותר. שיטה זו משמשת גם לסגירה של דלף נוזל מוח שידרתי (CSF) מהמח למערות הפנים, פתיחת דרכי הדמעות באנשים הסובלים מדמעת ודקומפרסיה (הורדת לחץ) ב Grave's ophtalmopathy (בלט של גלגלי העיניים ונזק לעצב הראיה בשל מחלת בלוטת התריס).
בעקבות הניסיון המצטבר התרחבו האינדיקציות וכיום מתבצעים ניתוחים אנדוסקופים לכריתת גידולי אף וסינוסים שפירים ובתנאים מסוימים אף כריתת גידולים ממאירים.
הדברים יכלו להיות פשוטים אלמלא האנטומיה המורכבת והקירבה של אזור האף ומערות הפנים לאיברים חיוניים כמו העיניים, המח ועורק התרדמה המוביל דם למח (Internal carotid artery). אומנם פגיעה כירורגית באיברים אלו נדירה, אולם כאשר היא מתרחשת עלול להיגרם נזק משמעותי. חששו של המנתח מפני סיבוכים קשים גורם לו לעיתים להימנע מהתקרבות לאזורים מסוכנים. זהירות זו מגנה מסיבוכים אך עלולה להיות כרוכה בהשארת מוקדי מחלה לא מטופלים.
לאנטומיה המורכבת מתלווה קושי נוסף המתבטא, ברב המקרים, ביכולת המצלמה האנדוסקופית לספק תמונה דו-ממדית בלבד, זאת בניגוד לתמונה תלת-ממדית, המתקבלת ממכשירים אחרים, דוגמת מיקרוסקופ. חיסרון זה מגביל את יכולת המנתח לקבל תחושת עומק ומחייב אותו להסתמך, לא אחת, על מדידת עומק חדירת כלי הניתוח וזווית כניסתו במטרה להעריך את מיקום קצהו.
במטרה לפתור קשיים אלו, רתמו מנתחי האף והסינוסים לשרותם אמצעי טכנולוגי חדיש ומתוחכם, המהווה פריצת דרך בהגברת יעילות ובטיחות הניתוחים האנדוסקופיים – מערכת מונחית דימות (Image-guidance system). באמצעות קרני איפרה אדום מאפשרת המערכת למנתח לצפות במיקומו המדוייק של קצה הכלי הניתוחי אותו הוא אוחז על גבי תצוגה תלת-מימדית של CT או MRI אותם ביצע המנותח טרם הניתוח (תמונה מס' 1).
תמונה מס' 1

שימוש במערכת זו מחייב הכרת מרכיביה ע"י צוות חדר הניתוח והכנה מתאימה של המנותח טרם מועד הניתוח. עם קביעת הצורך בניתוח מונחית דימות מופנה החולה לביצוע דימות (לרב CT ). ממצאי הבדיקה מועברים ברשת פנימית אל תחנת עבודה ממוחשבת, הנמצאת בחדר הניתוח. מול תחנת עבודה זו יכול המנתח לבדוק את איכות הסריקה ולבצע תכנון מדויק של הניתוח. לדוגמא: ניתן לסמן את היעד (מורסה או גידול) בצבע על מנת שבזמן הניתוח ניתן יהיה לאתר את מיקום כלי העבודה ביחס למטרה (תמונה מספר 2).
תמונה מס' 2

ניתן, גם,לאחד (fusion) הדמייתCT והדמיית MRI ולקבל תמונה ייחודית, המדגימה הן את המרכיבים הגרמיים והן את מרכיבי הרקמה הרכה בכל חתך.
כל המידע הממוחשב המתקבל מועבר לדיסק אשר מוזן ביום הניתוח למערכת מונחית הדימות, הממוקמת בחדר הניתוח.
לאחר הרדמת החולה וקיבוע ראשו, מתבצע תהליך רישום (registration) , אשר נועד לאחד במרחב את המידע התלת מימדי שבמחשב עם מיקום החולה הקונקרטי. בפועל, מתבצע הדבר ע"י סימון מדויק של פני החולה הנרשם באמצעות קרני אינפרה-אדום או חיישנים אלקטרומגנטיים.
לאחר מכן, מתבצע כיול ((calibration המערכת, קרי: הזנת מידות כלי הניתוח הספציפי בו נעשה השימוש ברגע נתון, כדי שקרני האינפרה-אדום או החיישנים האלקטרומגנטיים יוכלו לעקוב במדוייק אחר קצהו. במהלך הניתוח, מביט המנתח רב הזמן במוניטור המציג את המראה האנדוסקופי של שדה הניתוח. כאשר רוצה המנתח לוודא את מיקומו המדוייק בשדה הניתוח, יסיט את מבטו לצג מערכת הניווט אשר מסמן את מיקום קצה הכלי הניתוחי ב-3 מימדים נפרדים של CT (אקסיאלי,קורונלי וסגיטלי) ברמת סטיה של לא יותר מ-2 מ"מ. במידה רבה, ניתן להמחיש את עקרון פעולת המערכת ע"י השוואתה למערכות ה GPS המוכרות כיום לכולנו.
במאמר, המסכם 1000 מקרים של ניתוח סינוסים מונחה הדמיה (Image guided surgery), בעיתון: " Journal of Otolaryngolgy Head& Neck Surgery", נמצא כי השימוש במערכות ניווט מעלה את בטחונו של המנתח, בפרט בעת מיקרים קשים של היעדר סמנים אנטומיים בשל ניתוחים קודמים או מחלות נרחבות. עם זאת, המאמר הדגיש כי אין להתבסס על מערכת זו בעת ביצוע פעולות של מילימטר. זאת ועוד, כאשר קיימת סתירה בין המידע ממערכת הניווט למידע הקליני, על המנתח לפעול בהתאם לשיקוליו הקליניים ובכל מקרה, אין טכנולוגיה זו מהווה תחליף למיומנויות המנתח.
חשוב לציין כי מערכת הניווט מאפשרת ניתוח המונחה על פי הדימות שנעשה טרם הניתוח, ולכן, שינויים ברקמה הרכה או הקשה החלים עם התקדמות הניתוח אינם באים לידי ביטוי בתצוגת הניווט העומדת לרשות המנתח. לרב, חיסרון זה אינו משמעותי שכן האתגר העיקרי הוא להימנע מפריצת המעטפת הגרמית של האף והסינוסים, שבמרבית המקרים אינה משתנה בזמן הניתוח. עם זאת, לאור התרחבות האינדיקציות לניתוחים המערבים גם את החלל התוך-גולגלתי עולה הדרישה למערכת ניווט המספקת עדכון בזמן אמיתי. מענה לדרישה כבר נמצא בשלבי פיתוח של אמצעי ניווט בזמן אמיתי אשר כוללים MRI בעוצמת שדה נמוכה, CT נייד וגלי קול (U.S).
Recent Comments